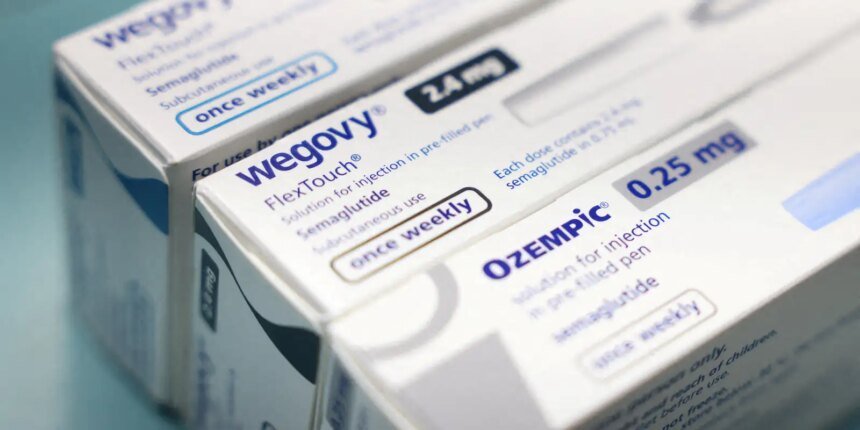
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou um robusto plano de ação para fortalecer o controle sanitário e coibir irregularidades na produção e comercialização de medicamentos injetáveis agonistas do receptor GLP-1, popularmente conhecidos como canetas emagrecedoras. As novas medidas visam proteger a saúde pública frente ao crescimento exponencial de produtos manipulados à base de ativos como semaglutida, tirzepatida e liraglutida, que têm sido alvo de preocupações regulatórias globalmente.
A iniciativa surge em resposta a um cenário de alarmante incompatibilidade entre o volume de Insumos Farmacêuticos Ativos (IFAs) importados e a real demanda do mercado, além de crescentes relatos de eventos adversos e práticas de uso indevido.
O Crescimento Exponencial e os Riscos da Manipulação Irregular
A Anvisa identificou um desequilíbrio notável na cadeia de suprimentos desses medicamentos. Somente no segundo semestre de 2025, o Brasil importou cerca de 130 quilos de IFAs relacionados a esses ativos, quantidade que seria suficiente para a preparação de 25 milhões de doses. Esse volume excede largamente a demanda estimada para manipulação individualizada, levantando suspeitas sobre a finalidade e a legalidade da produção.
Adicionalmente, um levantamento da agência em 2026 revelou sérias falhas em estabelecimentos do setor. Das 11 inspeções realizadas em farmácias de manipulação e importadoras, oito empresas foram interditadas devido a problemas técnicos e ausência de controle de qualidade, evidenciando a fragilidade das práticas em parte do mercado.
Preocupações com a Saúde e o Uso Indevido
Os riscos sanitários mapeados pela Anvisa são diversos e preocupantes. Eles incluem a produção sem previsão de demanda por manipulação, falhas críticas na esterilização de produtos injetáveis, deficiências nos processos de controle de qualidade e a utilização de insumos farmacêuticos sem identificação clara de origem e composição. A agência também registrou o uso indevido de nomes comerciais e a divulgação e venda de múltiplos produtos sem o devido registro.
A Anvisa tem observado um aumento nos relatos de eventos adversos e a proliferação do uso 'off-label' (prescrição diferente da aprovada em bula) desses medicamentos, especialmente para emagrecimento sem indicação clínica. Em fevereiro, a agência já havia emitido um alerta sobre o risco de pancreatite associado a essas canetas. Desde janeiro deste ano, dez ações de proibição de importação, comércio e uso de produtos irregulares contendo agonistas de GLP-1 já foram publicadas.
Estratégia Abrangente para a Segurança do Consumidor
O diretor-presidente da Anvisa, Leandro Safatle, esclareceu que as medidas implementadas não visam restringir o mercado ou proibir a manipulação dos ativos. O foco principal é coibir o uso irregular, assegurar a qualidade e eficácia dos produtos e, acima de tudo, proteger a saúde da população. Ele ressaltou que a situação representa um desafio regulatório global, com agências internacionais também buscando soluções para o consumo crescente e a manipulação desses medicamentos.
Aprimoramento Regulatório e Normativo
Um dos pilares do plano de ação é a revisão de normas cruciais. A Nota Técnica 200/2025, que orienta os procedimentos de importação, manipulação e controle sanitário de IFAs de agonistas de GLP-1, passará por uma atualização. A nova regulamentação cobrirá toda a cadeia produtiva, desde a entrada do insumo até o produto final, com especificações detalhadas sobre rastreabilidade, qualidade, segurança, qualificação de fabricantes e fornecedores, e testes mínimos de controle. Esta proposta será discutida em breve pela diretoria da agência.
Paralelamente, a resolução RDC 67/2007, que estabelece as boas práticas de manipulação para farmácias, também será revisada. Além disso, a Anvisa fortalecerá as medidas sanitárias cautelares, permitindo a suspensão da Autorização de Funcionamento (AFE) em casos de risco iminente à saúde e a retirada automática do efeito suspensivo de recursos administrativos, agilizando as ações de proteção.
Monitoramento e Fiscalização Intensificados
A Anvisa intensificará as ações de fiscalização, com foco em inspeções em importadoras, farmácias de manipulação e clínicas de estética. Será realizada uma busca ativa por eventos adversos relacionados a medicamentos manipulados, utilizando o sistema VigiMed, onde profissionais de saúde e cidadãos podem notificar ocorrências. O plano também prevê o aperfeiçoamento da matriz de risco para o controle sanitário da importação de IFAs e a ampliação das medidas preventivas para reprimir a entrada de produtos irregulares no país.
Articulação Institucional e Comunicação Transparente
A agência buscará acordos de cooperação técnica e a criação de grupos de trabalho com entidades médicas e outros órgãos de controle. Essa articulação federativa e internacional é essencial para uma abordagem coordenada. Adicionalmente, serão implementadas ações proativas de informação e treinamento, visando educar tanto profissionais de saúde quanto a população sobre os riscos e a importância da conformidade regulatória.
Conclusão: Compromisso com a Segurança do Paciente
O conjunto de medidas anunciadas pela Anvisa reflete um compromisso inequívoco com a segurança do paciente e a integridade do sistema regulatório farmacêutico. Ao abordar as complexidades do mercado de medicamentos agonistas de GLP-1 manipulados, a agência busca não apenas corrigir irregularidades, mas também estabelecer um ambiente de maior transparência e controle, garantindo que os produtos disponíveis no Brasil sejam seguros, eficazes e utilizados de maneira responsável. Essas ações são um passo fundamental para salvaguardar a saúde da população diante de um cenário de rápidas transformações e desafios no setor farmacêutico.