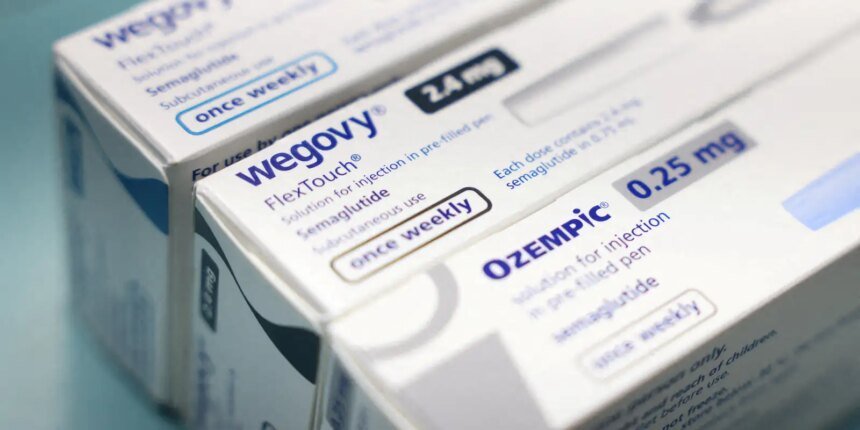
A partir desta sexta-feira, o mercado farmacêutico brasileiro se prepara para uma mudança significativa com a expiração da patente da semaglutida no país. Este princípio ativo, amplamente reconhecido como a base de medicamentos agonistas do receptor GLP-1 – popularmente conhecidos como 'canetas emagrecedoras', como o Ozempic –, encerra seu período de exclusividade, abrindo portas para a fabricação e comercialização de versões mais acessíveis. A medida promete democratizar o acesso a tratamentos importantes para o controle do diabetes tipo 2 e, em algumas indicações, para o manejo do peso.
Fim da Exclusividade e as Perspectivas para o Consumidor
A queda da patente da semaglutida é um marco que sinaliza o início de uma nova fase para o setor farmacêutico e, consequentemente, para milhões de pacientes. A substância, que se tornou um dos medicamentos mais procurados nos últimos anos devido à sua eficácia, agora poderá ser replicada por outros laboratórios. Essa concorrência tende a resultar em uma redução dos preços de mercado, tornando os tratamentos mais viáveis e ampliando o número de pessoas que podem se beneficiar de seus efeitos terapêuticos. A expectativa é que essa movimentação no mercado estimule a inovação e aprimore o acesso a soluções de saúde.
Anvisa em Análise: Oito Pedidos de Registro em Andamento
Diante da iminente expiração da patente, a Agência Nacional de Vigilância Sanitária (Anvisa) já registra uma intensa atividade. Atualmente, há oito processos em fase de análise para o registro de novos medicamentos contendo o mesmo princípio ativo. Destes, dois pedidos de registro de semaglutida sintética estão em 'exigência', dependendo da apresentação de dados complementares pelas empresas, com prazo para resposta até o final de junho. No campo dos produtos biológicos, um está sob análise e outro aguarda o início de sua avaliação. A agência prevê que os demais pedidos receberão um posicionamento técnico – que pode ser de aprovação, reprovação ou nova exigência – até o fim de abril, indicando a celeridade do processo regulatório.
Desafios Técnicos na Avaliação de Análogos Sintéticos
A complexidade da semaglutida impõe um desafio técnico significativo para a Anvisa e outras agências reguladoras globais. Os medicamentos atualmente registrados no Brasil são classificados como produtos biológicos. No entanto, os novos pedidos em avaliação abrangem tanto biossimilares (obtidos por via biológica) quanto análogos sintéticos de peptídeos biológicos (obtidos por síntese química). Para esses últimos, não existe a opção de registro como genéricos ou similares no sentido tradicional, exigindo uma abordagem de avaliação única. Até o momento, as principais agências internacionais, como as do Japão, Europa e Estados Unidos, não registraram análogos sintéticos de semaglutida, sublinhando a vanguarda e a complexidade desta análise no Brasil.
A Dupla Natureza da Avaliação Regulamentar
A avaliação dos análogos sintéticos de semaglutida é particularmente desafiadora devido à sua natureza híbrida. Esses produtos combinam preocupações típicas de fármacos sintéticos, como a presença de resíduos de solventes, catalisadores metálicos e impurezas químicas, com as de produtos biológicos, que incluem o risco de imunogenicidade (a formação de respostas imunes indesejadas) e a agregação de moléculas. A Anvisa precisa conciliar ambos os conjuntos de parâmetros rigorosos para garantir que os novos medicamentos sejam tão seguros e eficazes quanto o produto de referência, assegurando a integridade e a resposta biológica desejada em pacientes.
Segurança e Eficácia: Os Principais Focos da Anvisa
Para garantir a segurança do paciente e a eficácia terapêutica, a Anvisa concentra sua atenção técnica em pontos cruciais durante a avaliação dos novos produtos. Entre eles, destacam-se a análise de impurezas, a propensão à formação de agregados, a garantia de esterilidade e, fundamentalmente, a imunogenicidade. O objetivo primordial é assegurar que o medicamento não induza reações imunes adversas, como a produção de anticorpos anti-fármaco, que poderiam não apenas comprometer a eficácia de qualquer formulação de semaglutida para o paciente, mas também desencadear reações imunológicas mais severas. Essa vigilância rigorosa visa proteger a saúde pública enquanto novos tratamentos são introduzidos no mercado.
Decisão do STJ Reafirma Limite da Patente
Em janeiro, uma decisão do Superior Tribunal de Justiça (STJ) já havia solidificado o cenário da expiração da patente da semaglutida. A Quarta Turma do STJ negou o pedido de prorrogação do prazo de vigência das patentes do Ozempic e do Rybelsus (outro medicamento com semaglutida, em formato oral), ambos detidos pela empresa dinamarquesa Novo Nordisk. A ação foi movida pela Novo Nordisk contra o Instituto Nacional da Propriedade Industrial (INPI), buscando reconhecimento por alegada demora administrativa na tramitação das patentes. No entanto, as instâncias ordinárias e o STJ mantiveram o entendimento, baseado na Ação Direta de Inconstitucionalidade 5.529 do Supremo Tribunal Federal (STF), de que o prazo de vigência de uma patente de invenção é inegociável: 20 anos a partir do depósito do pedido no INPI, sem possibilidade de prorrogação judicial por atrasos administrativos. Essa decisão reforça a previsibilidade e a segurança jurídica no sistema de patentes brasileiro.
O Futuro da Semaglutida no Brasil
A expiração da patente da semaglutida marca o início de uma nova era para o acesso a este importante medicamento no Brasil. Com a abertura do mercado para versões mais acessíveis, espera-se um impacto positivo na saúde pública, permitindo que um número maior de pacientes se beneficie de tratamentos eficazes para o diabetes e o controle de peso. A Anvisa, por sua vez, desempenha um papel crucial na garantia de que os novos produtos mantenham os mesmos padrões rigorosos de segurança e eficácia, navegando os complexos desafios técnicos que envolvem a avaliação de análogos sintéticos. A combinação do fim da exclusividade e da vigilância regulatória promete transformar o cenário da semaglutida, equilibrando inovação com acessibilidade.